新技術情報
このページでは、当社が共同研究などを通じて開発した新規技術を紹介します。
・免疫-質量分析法(Immuno-MS)による血清α-Fetoproteinの定量分析
・Phos-tag対角線電気泳動
血清マーカータンパク質の定量分析
免疫-質量分析法(Immuno-MS)による血清α-Fetoproteinの定量分析
Immuno-MSは、免疫沈降法 (Immunoprecipitation, IP) と質量分析 (Mass spectrometry, MS) を組み合わせた手法であり、IP-MSとも呼ばれています。分析対象タンパク質(抗原)を抗体との反応性を利用して精製するため(アフィニティ精製)、生体試料に含まれる微量タンパク質の分析に威力を発揮します。当社では、肝臓癌の血清マーカーの一つであるα-fetoprotein (AFP) を対象にしてImmuno-MSによる定量分析の手順を整備しました。多摩川精機株式会社との共同研究です(Takahataら、2023年; PMID: 37260735)。
AFPはこんなタンパク質です。
・胎児の肝細胞や卵黄嚢で産生
・誕生後に血清アルブミンに代替
・分子量約70万
・肝細胞癌や精巣腫瘍の腫瘍マーカー(図1)
・iPS細胞などの分化の状態を示すマーカーとしても広く利用されています。
図1.肝癌マーカー、α-fetoprotein (AFP)
定量分析系の構築にあたって、抗AFP抗体を磁性粒子に固定化しました(図2)。
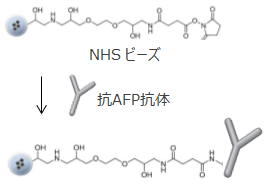
図2.抗AFP抗体の固定化
固定化反応はリンカー分子による共有結合を介しておこないました。この固定化の様式は、Protein A/Gを用いた方法に比べて抗原と抗体を分離しやすい点で有利です。
固定化抗体を用いて、血清にAFPの組み換え体を一定量添加したモデル試料からAFPをアフィニティ精製しました。抗体固定化のための磁性粒子を多摩川精機のFG beads®と他社製品との間で比較したところ、FG beadsの方が非特異的な結合が少ないことが分かりました(図3)。
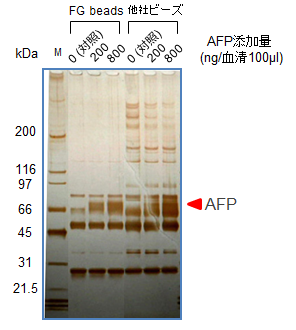
図3.アフィニティ精製試料のSDS-PAGE
磁性粒子に固定化した抗AFP抗体を用いてImmuno-MSの工程を整備しました(図4)。
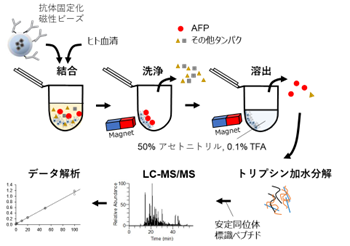
図4.Immuno-MSの工程
本工程では、血清からアフィニティ精製したAFPを固定化抗体から分離回収したあとに、トリプシンによる加水分解に供しました。LC-MS/MSによるAFP由来ペプチドの定量測定は、既知量を添加した安定同位体標識ペプチドの検出強度を指標にしました。
一般にImmuno-MSは、微量の抗原分子から当該分子由来のペプチド断片を特異的かつ効率的に回収することが重要です。ペプチド回収までの工程は、抗原タンパク質を固定化抗体に結合したまま加水分解する方法と、加水分解の前に抗原を固定化抗体から溶出、回収する手順(溶出後加水分解)に大別されます。本研究では後者の条件を最適化しました。抗体をあらかじめ磁性粒子に共有結合しているので抗原と抗体の分離が容易であり、このため抗体由来の分解ペプチドの混入を低減することができます。
分析手順の最適化にあたっては、抗原AFPの溶出液の組成を比較検討しました。その結果、0.1%TFAで酸性にした50%アセトニトリル水溶液で溶出した場合にAFPの回収率が最も高く(図5)、かつ固定化抗体に結合したまま加水分解するよりも高い計量値が得られました。
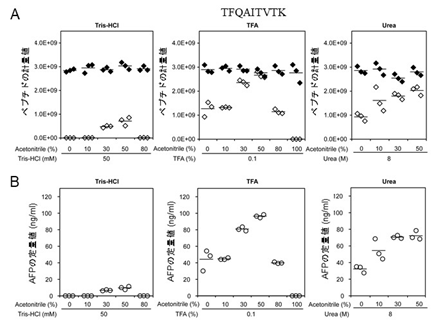
図5. 溶出液の組成の最適化
AFP由来ペプチド断片のひとつ、TFQAITVTKの測定結果を示しました。
血清に添加したAFP標品を、固定化抗体を用いて精製。その後、溶出液
中に回収したAFPをトリプシン加水分解に供しました。各条件ともに3複製。
(A) ペプチドの計量値(検出強度)
◇: 抗原AFP由来
◆: 既知量添加した安定同位体標識体
(B)標識体の検出強度を指標に算出したAFP濃度
この溶出液を用いて定量性を検討したところ、添加したAFP標品の濃度範囲0~100 ng/mLにおいて高い検出直線性を示しました(R2 > 0.996)(図6)。また、検量線の回帰式を用いて内在性の血清AFPの濃度を算出したところ、2.3~2.4 ng/mLの値が得られました。この定量値は、既報の標準ヒト血清中の濃度範囲(10 ng/mL未満)にも整合しています。
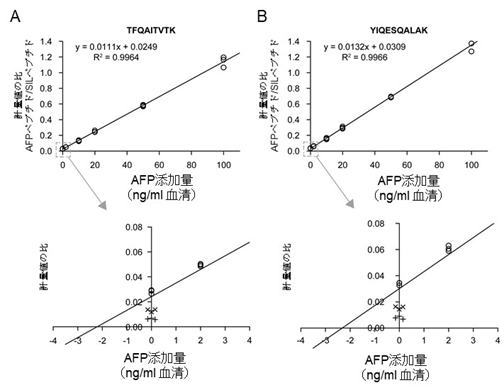
図6.定量性の評価
AFP由来ペプチド断片のうち、TFQAITVTK (A)およびYIQESQALAK (B)
を評価の対象としました。
Immuno-MSでは、交差反応性を持つ抗原をMSで区別することが可能です。このため、翻訳後修飾の分析やアイソフォームの個別定量にも適しています。
今後は、本研究で構築した定量分析手順を他のマーカータンパク質に適用し、手順の有用性を確かめる予定です。また、磁性粒子の特性を生かした分析工程の自動化や多試料の同時調製も検討していきます。
2023年6月2日更新
Phos-tagの応用
Phos-tag対角線電気泳動
当社は、プロテオーム解析に必要な新しい技術の開発、改良研究の成果に特別な関心を持っています。これから当社の研究結果を含め、新しい技術情報をみなさまにご紹介していきたいと考えております。第1回は、Phos-tag対角線電気泳動に関する話題です。
ショットガン分析の発達により、生体試料中の多種類のタンパク質を比較定量的に同定できるようになりました。リン酸化タンパク質についても同様です。培養細胞では、1回の分析で、2千種類ほどのリン酸化タンパク質、4〜6千のリン酸化部位の同定も困難ではなくなりました。しかし、ショットガン分析では、リン酸化タンパク質やリン酸化部位を同定できるのですが、同じタンパク質にリン酸化状態の異なるタンパク質が存在する場合には、その違いを解明できないことがあります。ショットガン分析では、質量分析の前にタンパク質をプロテアーゼによって断片化してしまうため、その情報が失われてしまうからです。
Kinoshitaら(2008)によって開発されたPhos-tag SDS-PAGEは、ショットガン分析で明らかにできないリン酸化状態の異なる分子の解析が行える画期的な方法です。しかし、この方法では解決したい課題がありました。タンパク質のリン酸化状態を分析する際には、同一試料をSDS-PAGEとPhos-tag SDS-PAGEで別々に分析します。そのため、SDS-PAGEでもPhos-tag SDS-PAGEでも単一のタンパク質バンドが検出された場合、Phos-tag SDS-PAGEで易動度が変化したのかどうか判定することが困難でした。また、Phos-tag SDS-PAGEで複数のタンパク質バンドが検出された場合には、易動度が明らかに低下しているバンドはリン酸化されていることが判定できるのですが、易動度が最も大きいバンドの易動度がPhos-tagによって変化しているのかどうかは簡単に判断できませんでした。そのため、この問題を解決できる簡便な技術の開発が必要でした。
当社は、平野 久、木下英司両博士らと共同で、上記の課題を解決できるPhos-tag対角線電気泳動を開発しました(Okawaraら2021)。一次元目にSDS-PAGE、二次元目にPhos-tag SDS-PAGEを用いたこの方法は、非リン酸化タンパク質を対角線上に、リン酸化タンパク質を対角線より陰極側に分離することができます。分離されたスポットをMS/MSで解析すれば、タンパク質を同定することもできますし、同じタンパク質として同定された異なるスポットのリン酸化部位の違いを解明できる可能性もあります。
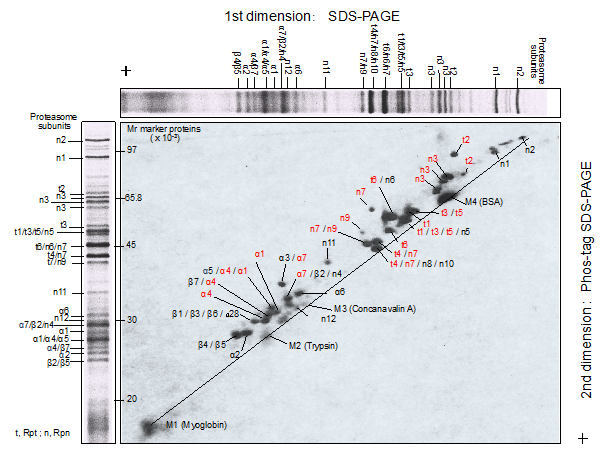
ヒト26SプロテアソームサブユニットのPhos-tag対角線電気泳動パターン(Okawaraら2021)
図は、ヒト26SプロテアソームサブユニットをPhos-tag対角線電気泳動を用いて分離してみた結果です(分離能の高さにご注目下さい)。分離されたスポットは切り取ってエッペンドルフチューブ中でトリプシンを用いてゲル内消化を行った後、LTQ-Orbitrap MSによって分析し、MS/MSデータに基づいてデータベースを検索してサブユニットを同定しました。Phos-tag対角線電気泳動の対角線上のスポットはリン酸化されない対角線マーカータンパク質です。同定されたすべてのプロテアソームサブユニットは対角線の上方に検出されています。つまり、リン酸化されていることを示しています。また、サブユニットの中には、複数のリン酸化状態が存在することを示すスポットが検出されています。
当社では、これまでのショットガン分析によるリン酸化タンパク質やリン酸化部位の受託分析と共に、Phos-tag SDS-PAGEやPhos-tag対角線電気泳動を用いたタンパク質のリン酸化状態の受託分析も行うことができるように準備を進めています。
2021年5月6日掲載
上記技術に関するお問い合わせはこちらから
















